Ámsterdam:
El organismo de control de medicamentos de Europa aprobó parcialmente el jueves una solicitud de comercialización para un nuevo tratamiento largamente esperado para la enfermedad de Alzheimer, revocando una decisión anterior de no darle luz verde.
“Después de reexaminar la opinión inicial, la EMA… ha recomendado la autorización de comercialización de Lekambi (lecanemab) para el tratamiento del deterioro cognitivo leve o de la demencia leve debida a la enfermedad de Alzheimer”, dijo la Agencia Europea de Medicamentos, añadiendo que el tratamiento Sólo se aplica a un grupo específico de pacientes.
Lekambi, fabricado por la multinacional estadounidense Biogen y la japonesa Isai, es la marca de una sustancia activa llamada lecanemab, que se utiliza para tratar problemas cognitivos resultantes de la pérdida leve de memoria y las primeras etapas de la demencia en adultos.
La EMA rechazó una solicitud de comercialización en julio, diciendo que los efectos secundarios, incluido un posible sangrado cerebral, superaban los beneficios.
La EMA ha aprobado ahora el tratamiento, pero sólo para pacientes con bajo riesgo de hemorragia cerebral: aquellos que tenían “sólo una copia o ninguna copia de ApoE4”, un tipo de gen conocido por ser un importante factor de riesgo para el Alzheimer.
La EMA, con sede en Ámsterdam, dijo que estos pacientes tenían menos probabilidades de experimentar problemas de salud graves que aquellos con dos copias del gen.
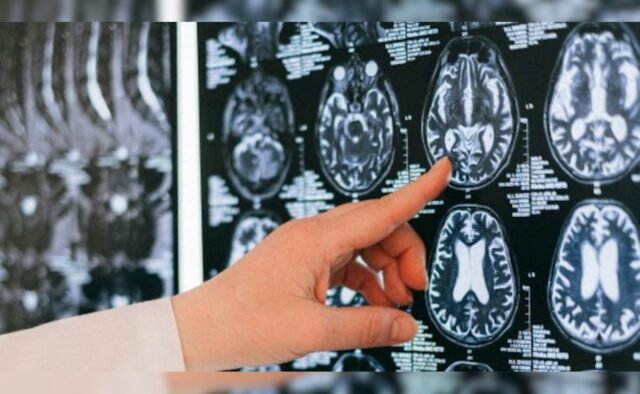
Los problemas de salud en cuestión, conocidos como anomalías de las imágenes relacionadas con el amiloide (ARIA), incluyen líquido en el cerebro y hemorragia cerebral.
“Los beneficios de Lekambi superan los riesgos en pacientes con deterioro cognitivo leve o demencia leve debido a la enfermedad de Alzheimer con una o ninguna copia de ApoE4”.
Esto “siempre que se apliquen medidas de reducción del riesgo para reducir el riesgo de ARIA grave y sintomática y controlar sus consecuencias a largo plazo”, subrayó.
Minimizar los riesgos incluye “controlar los programas de acceso para garantizar que el medicamento se use sólo en los pacientes recomendados” y realizar resonancias magnéticas antes y durante el tratamiento.
La aprobación de la EMA, con sede en Ámsterdam, se enviará ahora a la Comisión Europea para que tome una decisión final sobre su lanzamiento en el continente.
El precio y el reembolso quedarán en manos de los estados miembros, dijo la EMA.
Lecanemab ha sido aclamado por investigadores y organizaciones benéficas sobre el Alzheimer como el primer tratamiento aprobado que aborda las primeras etapas de la enfermedad en lugar de controlar los síntomas.
Funciona mediante el uso de anticuerpos que se unen y eliminan proteínas que normalmente se acumulan en el cerebro de personas con Alzheimer, el tipo más común de demencia.
Se ha demostrado que el tratamiento reduce el deterioro cognitivo en una cuarta parte en personas que se encuentran en las primeras etapas de la enfermedad.
El regulador de medicamentos de Gran Bretaña aprobó lecanemab en agosto, convirtiéndolo en el primer tratamiento autorizado de este tipo en el país.
Lakembi, junto con otro fármaco contra el Alzheimer llamado Aduhelmin, recibió la aprobación de la Administración de Alimentos y Medicamentos de EE.UU. a principios del año pasado.
(A excepción del titular, esta historia no fue editada por el personal de NDTV y apareció en un canal sindicado).